近日,陈航姿副教授和吴乔教授研究团队在《Cancer Research》杂志上在线发表了题为“Flightless-I blocks p62-mediated recognition of LC3 to impede selective autophagy and promote breast cancer progression”的研究论文。该研究工作揭示了Flightless-I蛋白抑制选择性自噬调控乳腺癌发生发展的机制。
选择性自噬是细胞以自噬的方式选择性清除受损的蛋白或细胞器的过程,作为细胞的质量控制系统在细胞稳态的维持中发挥重要作用,选择性自噬失调则可能造成肿瘤的发生。p62是最主要的自噬受体之一,介导多种选择性自噬过程,但哪些上游因子参与以及如何调控p62的功能却很不清楚。在本研究中,该团队通过免疫共沉淀和质谱分析首先发现了一个p62的新结合蛋白Flightless-I (FliI)。FliI是一个actin结合蛋白,因其突变可导致果蝇飞行肌发育异常,故而得名。但其与选择性自噬的关系并没有报道。研究表明FliI通过与p62结合抑制LC3对p62的识别,从而阻断p62介导的选择性自噬,进而导致细胞内受损蛋白和DNA的累积。进一步分析发现FliI的功能可被ULK1和Akt诱导的磷酸化双向调控:ULK1的磷酸化削弱了FliI对p62功能的抑制,从而促进选择性自噬进程;而Akt的磷酸化则增强FliI与p62的结合,抑制选择性自噬进程。由于选择性自噬与肿瘤的发生密切相关,该团队进一步在乳腺癌小鼠肿瘤模型中发现,敲除FliI可以促进选择性自噬、降低受损蛋白和受损DNA的水平,抑制乳腺癌的发生发展。在临床乳腺癌标本中,FliI在癌组织中的表达显著高于癌旁组织,且FliI的表达水平与乳腺癌的预后呈负相关。同时,ULK1对FliI的磷酸化水平在癌旁组织显著高于癌组织,而Akt对FliI的磷酸化水平则在癌组织中更强。
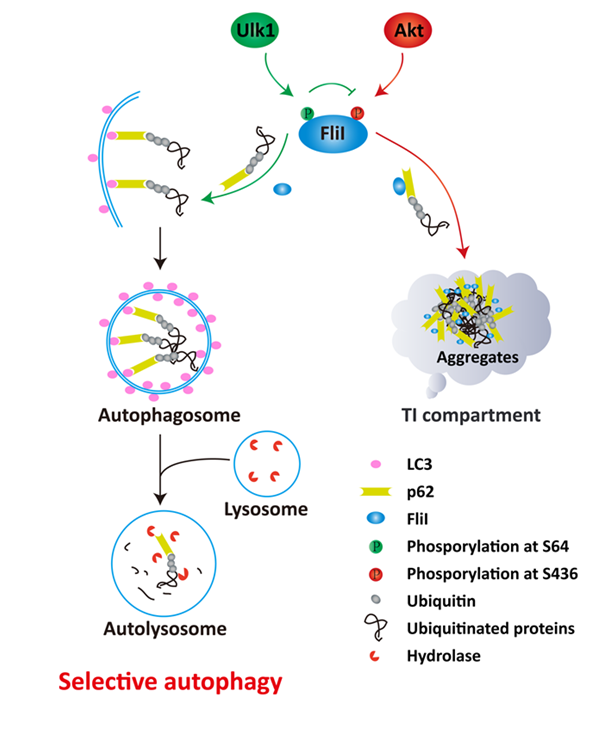
论文模式图
该研究不仅提出FliI作为选择性自噬的checkpoint protein负调控选择性自噬的机制,也提示靶向选择性自噬有望用于乳腺癌的治疗。该论文的共同第一作者为博士后何建平、博士生侯佩佩、陈旗涛,通讯作者为陈航姿副教授。该研究工作得到了国家自然科学基金、国家重点基础研发计划以及厦门大学校长基金的支持。
论文链接:http://cancerres.aacrjournals.org/content/early/2018/06/13/0008-5472.CAN-17-3835